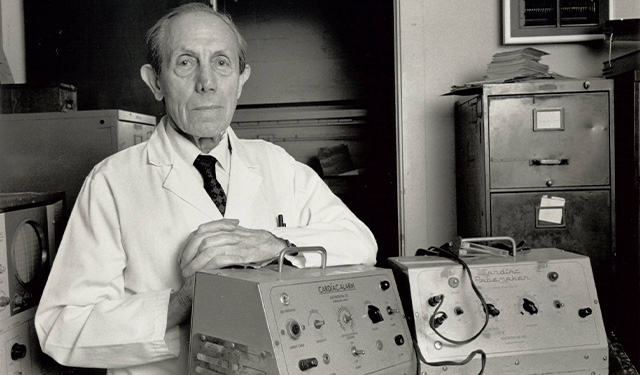
Dr. Paul M. Zoll
Las primeras investigaciones
1952
Siendo jefe del Servicio de Cardiología en el Hospital Beth Israel, el Dr. Paul M. Zoll demuestra que la estimulación eléctrica externa del tórax del paciente durante una parada cardíaca podría provocar un latido efectivo.
1956
El Dr. Zoll es el primer médico en usar con éxito la desfibrilación externa para regular el ritmo cardíaco de los pacientes. Este descubrimiento contribuyó de manera significativa al descenso de la mortalidad por causas cardíacas.
Con colaboradores técnicos, el Dr. Zoll desarrolla un método para mostrar la actividad cardíaca eléctrica del corazón en una pantalla osciloscópica. Esto lleva al desarrollo de monitores cardíacos y otros programas que se encuentran en las unidades coronarias modernas.
1960
El Dr. Zoll descubre que la cardioversión eléctrica externa es eficaz para interrumpir la taquicardia supraventricular y la taquicardia ventricular. Se extiende el uso de esta intervención en el tratamiento de estas arritmias y se comprueba que es más seguro que administrar grandes dosis de agentes antiarrítmicos.

1964
El Dr. Zoll desarrolla un método para la estimulación eléctrica directa a largo plazo mediante un marcapasos implantado.

1973
El Dr. Zoll recibe el Premio Albert Lasker de Investigación Médica Clínica, el premio más codiciado en la ciencia médica.
Foto cortesía de laskerfoundation.org
1977
El Dr. Zoll se convierte en catedrático médico emérito de la facultad de medicina de Harvard.
ZOLL Medical Corporation
1980
ZOLL® es constituida por los cofundadores de la empresa, entre los que se incluyen el Dr. Zoll, Leigh Stein y Thomas Claflin. Posteriormente se incorporan a ZOLL William Bright, presidente, y Rolf Stutz, director general.
1983
Se presenta el ZOLL NTP® 1000, un marcapasos temporal no invasivo desarrollado a partir de las investigaciones del Dr. Zoll.
1988
Lanza el marcapasos/desfibrilador/monitor ZOLL PD 1200™, la primera tecnología que combina electroestimulación cardíaca y desfibrilación en una unidad compacta, fiable y fácil de usar.
1989
Presenta los electrodos multifunción para adultos, que proporcionan una electroestimulación cardíaca con buena tolerancia, una desfibrilación eficaz, cardioversión y monitorización.
1992
ZOLL se convierte en una empresa pública.
Lanza el marcapasos/desfibrilador/monitor PD 1400, el aparato más pequeño y ligero de su clase disponible para el traslado de pacientes graves y el tratamiento prehospitalario.
La Asociación Estadounidense de Cardiología eleva la estimulación cardíaca no invasiva a tratamiento inicial de elección para algunas enfermedades graves. ZOLL es líder del mercado en esta tecnología.
1994
Recibe la autorización de venta 510(k) de la FDA para el desfibrilador externo automatizado (DEA)/desfibrilador asesor PD/D 2000.
1995
Establece una filial en Holanda.
Lanza ZOLL 1600, el primer desfibrilador externo manual/DEA actualizable y configurable.
Introduce el primer cargador de batería/fuente de alimentación de CA modular para uso hospitalario en las series de desfibriladores de ZOLL 1400, 1600 y 2000.
1996
Adquiere Westech Mobile Solutions e incorpora productos de información basados en software a la línea de productos prehospitalarios.
Hace una inversión de capital en LIFECOR, Inc., la empresa de equipos médicos que fabrica LifeVest®, el único desfibrilador para llevar puesto.
Introduce el ZOLL 1700, el primer desfibrilador externo manual/DEA totalmente integrado para soporte vital básico (SVB) y soporte vital avanzado (SVA) en un hospital.
Anuncia el nuevo Base PowerCharger™ 4 x 4, el primer sistema en el sector que ofrece una solución práctica para mejorar la fiabilidad, la eficacia y el coste del mantenimiento de las baterías.
1997
Lanza RescueNet®, el único sistema completo de gestión de la información de SME que ayuda a mejorar la atención a pacientes, la eficiencia operativa y el cumplimiento de la normativa.
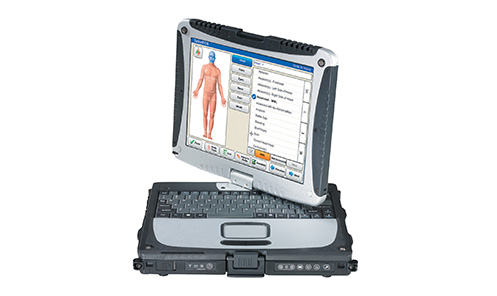
Presenta un sistema informatizado de ECG de 12 derivaciones con acceso desde una tableta que ayuda a identificar el inicio de una parada cardíaca.
1998
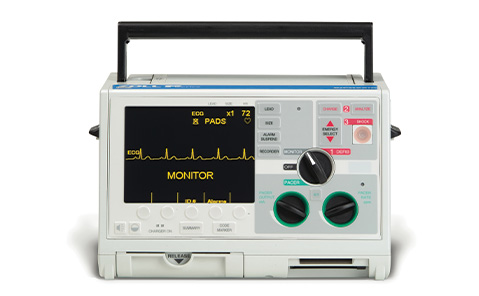
Presenta el desfibrilador/monitor M Series®, el desfibrilador más avanzado del mundo. Su tamaño es aproximadamente un tercio del de otros desfibriladores del mercado que incluyen todas las funciones y su peso es casi la mitad.
1999
Establece filiales en Canadá y Alemania.
Presenta la forma de onda de desfibrilación Rectilinear Biphasic™ y recibe la autorización de la FDA para etiquetar esta tecnología como clínicamente superior a los desfibriladores monofásicos para la conversión de la fibrilación ventricular en pacientes con alta impedancia y para la cardioversión de la fibrilación auricular.
Adquiere Pinpoint Technologies para ofrecer una solución completa de gestión de la información en el mercado de los SME.
Presenta las baterías inteligentes, una primicia en el sector que permite a los usuarios visualizar de forma precisa del tiempo de funcionamiento.
2001
ZOLL establece filiales en Australia y Francia.
Lanza M Series CCT para el transporte de pacientes de cuidados intensivos.
Se diseña el desfibrilador ZOLL AED Plus® en colaboración con cientos de reanimadores y centros de SME.
2002
Recibe la autorización de venta 510(k) de la FDA para su desfibrilador AED Plus y los nuevos electrodos CPR-D-padz®, el primer sistema que proporciona información instantánea sobre la profundidad y frecuencia de las compresiones torácicas durante la RCP.
ZOLL concede una primera subvención para ayudar a establecer la AED Instructor Foundation (Fundación para Instructores de DEA).
ZOLL y LIFECOR, Inc. anuncian un acuerdo para vender a hospitales el desfibrilador para llevar puesto LifeVest de LIFECOR para su uso en pacientes en Estados Unidos y Canadá.
El M Series CCT es elegido como el desfibrilador de preferencia del U.S. Military Patient Movement Item Program (Programa de Artículos para Movimiento de Pacientes Militares de los EE. UU.). El contrato, por un valor de 8,9 millones de dólares, constituye el mayor pedido en la historia de ZOLL.
2003
Anuncia una colaboración con Advanced Circulatory Systems, Inc. para lanzar al mercado el dispositivo de mejora de la circulación ResQPOD®.
Llega a un acuerdo con Revivant Corporation para comercializar la bomba no invasiva de reanimación cardíaca AutoPulse®, un aparato portátil aprobado recientemente por la FDA que automatiza las compresiones torácicas y aumenta la circulación sanguínea al cerebro y al corazón de manera más estable que la RCP manual.
2004
Establece una filial en Austria.
Cambia el nombre de Pinpoint Technologies por ZOLL Data Systems para representar mejor el mercado de los SME.Adquiere Infusion Dynamics, Inc., fabricante de un producto único para la reanimación con líquidos llamado Power Infuser®.
La función pediátrica del AED Plus recibe la autorización de la FDA.
2005
Presenta el ZOLL AED Pro® para reanimadores profesionales.
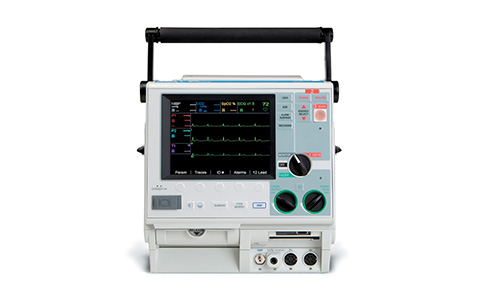
Lanza el monitor/desfibrilador E Series®, diseñado para cumplir con las exigencias específicas y las condiciones extremas del entorno de los SME.
2006
Completa la adquisición de los activos de LIFECOR, Inc.
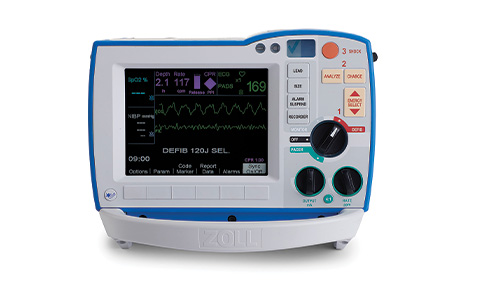
Lanza el monitor/desfibrilador R Series®, el único desfibrilador con tecnología Code-Ready® para hospitales.
2007
Recibe la autorización de venta para el E Series con tecnología Real CPR Help®.
Adquiere los recursos de control de la temperatura de Radiant Corporation.
Supera los 300 millones de dólares en ingresos.
Recibe la autorización de venta para el E Series y AED Pro con tecnología See-Thru CPR®, una función que ayuda a reducir las interrupciones durante la RCP.
2008
Las soluciones para el IAMCEST ofrecen una tecnología de transmisión mejorada para los ECG de 12 derivaciones.
Se aprueba el uso del AED Pro en helicópteros de evacuación sanitaria, al recibir la certificación de que cumple los criterios del Ministerio de Defensa de EE. UU. para los productos sanitarios tras las exhaustivas pruebas realizadas por el Laboratorio de Investigación Aeromédica del Ejército de EE. UU.
Se aprueba el uso de AutoPulse en China.
El desfibrilador para llevar puesto LifeVest supera las 10 000 prescripciones.
ZOLL y Welch Allyn acuerdan una alianza estratégica: ZOLL se convierte en distribuidor exclusivo de Propaq® LT.
Alcanza los 398 millones de dólares de ingresos, lo que supone un aumento del 29 % respecto al año anterior.
2009
Adquiere los recursos de control de la temperatura intravascular (IVTM™) de Alsius Corporation.
Los nuevos desfibriladores/monitores R Series BLS y R Series Plus reciben la autorización de la FDA.
2010
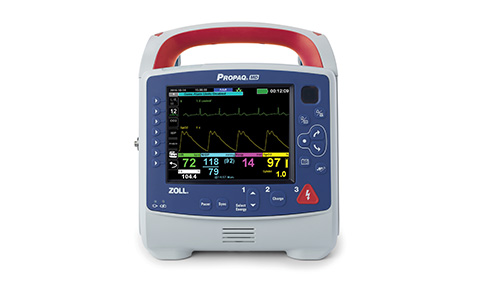
El monitor/desfibrilador Propaq MD y el monitor Propaq M obtienen la autorización de la FDA.
Se alcanzan las 30 000 prescripciones de desfibriladores para llevar puestos LifeVest.
2011
El ensayo AutoPulse CIRC (circulación para mejorar el tratamiento de reanimación) concluye con éxito; es el primer estudio a gran escala sobre reanimación en el cual se obtienen resultados estadísticamente significativos.
Recibe el premio de liderazgo en el mercado de Frost & Sullivan 2010 por su excelencia demostrada en la captación de la mayor cuota de mercado en EE. UU. en el sector de los desfibriladores externos.
PocketCPR® para iPhone, una aplicación de formación, es la primera en respaldar las nuevas directrices de la AHA, ERC e ILCOR de 2010.
ZOLL notifica ingresos y ganancias récord en el cuarto trimestre y en el año; supera la barrera de los 500 millones de dólares con unos ingresos de 523,7 millones en el año fiscal de 2011.

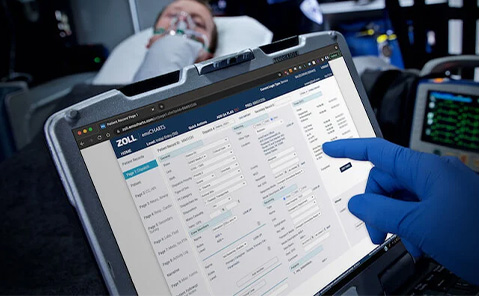
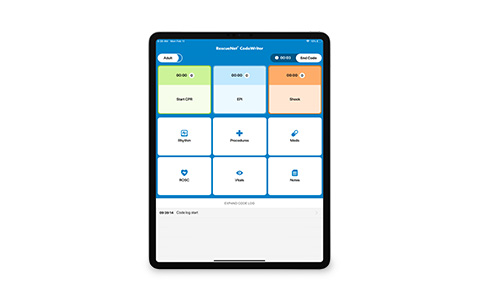
Lanza la aplicación para iPad de historias clínicas electrónicas; los equipos de los SME ahora pueden usar la tecnología de iPad para rellenar de manera electrónica las historias clínicas de los pacientes.
2012
Asahi Kasei adquiere ZOLL por 2210 millones de dólares.
ZOLL presenta los primeros electrodos de uso pediátrico que informan de la calidad de la RCP en niños de hasta ocho años.
ZOLL establece la nueva filial japonesa Asahi Kasei ZOLL Medical (AZM).
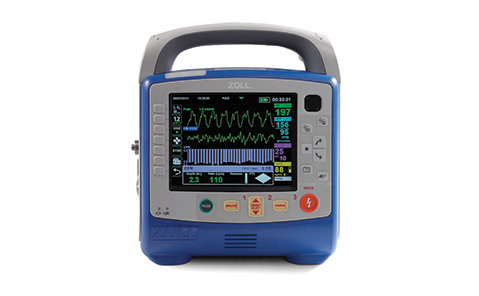
El monitor/desfibrilador X Series® recibe la autorización 510(k) de la FDA.
2013
Primera empresa de dispositivos médicos en firmar el compromiso de poner a disposición de los médicos datos de los pacientes en tiempo real, por ejemplo, desde los SME hasta los hospitales, con el fin de reducir las muertes evitables.
Presenta el AED Plus completamente automático con Real CPR Help, que administra automáticamente una descarga cuando detecta un ritmo cardíaco desfibrilable.
2014
Amplía su cartera de productos para incluir dispositivos de ventilación con la adquisición de los recursos de Impact Instrumentation, Inc.
Adquiere el negocio de control de la temperatura InnerCool® de Philips.
2015
Adquiere Advanced Circulatory Systems, Inc., de Roseville, Minnesota (EE. UU.), la empresa que desarrolló ResQPOD.
La FDA otorga la aprobación previa a la comercialización al sistema ResQCPR®, tras comprobarse en estudios preclínicos que aumenta significativamente el flujo sanguíneo al corazón y a otros órganos vitales.
2016
ZOLL recibe la autorización para comercializar en Japón su tecnología de control de la temperatura intravascular para tratar las paradas cardíacas súbitas.
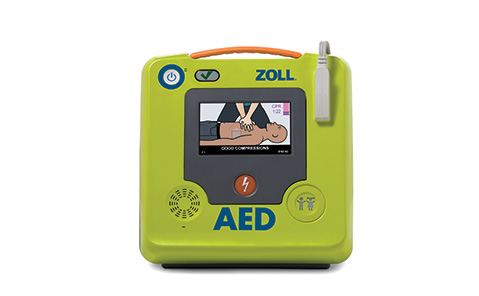
Se aprueba la comercialización y distribución en Europa de los desfibriladores externos automáticos ZOLL AED 3® y ZOLL AED 3 BLS.
Se crea la beca ZOLL EMT, que se otorgó a once cuidadores en el primer año del programa.
2017
Health Canada aprueba los desfibriladores externos automáticos ZOLL AED 3 y ZOLL AED 3 BLS para su comercialización y distribución en Canadá.
El desfibrilador hospitalario para llevar puesto recibe la aprobación previa a la comercialización de la FDA.
2018
Las Fuerzas Aéreas y del ejército de EE. UU. eligen Propaq M como su monitor de signos vitales para despliegues.
ZOLL se convierte en la primera empresa que recibe la aprobación previa a la comercialización de la FDA para su gama completa de desfibriladores.
El ensayo VEST muestra que el desfibrilador para llevar puesto LifeVest reduce la mortalidad total en un 36 % tras 90 días.
Se lanza el programa Heroes for Life para rendir homenaje a los supervivientes de parada cardíaca súbita y los «héroes inesperados» que ayudaron a salvarlos con un DEA de ZOLL.
Se presenta la aplicación Respond™ para mejorar la comunicación y la navegación entre teleoperadores de urgencias médicas, equipos y personal médico.

Se presenta el ventilador de transporte Z Vent® para uso prehospitalario y hospitalario.
2019
Adquiere Payor Logic, Inc., empresa especializada en soluciones avanzadas de software de cobros pendientes para la industria sanitaria.
Adquiere Golden Hour Data Systems, Inc. Acelera la redacción de la historia clínica del paciente y la gestión del ciclo de ingresos para el mercado de los SME.
Presenta el sistema de control de insuficiencias cardíacas y arritmias µCor™ (pronunciado «micro core»), una nueva tecnología para mejorar el tratamiento de pacientes con insuficiencia cardíaca aguda.
Adquiere TherOx®, Inc., que ofrece la terapia de oxígeno sobresaturado (SSO2), un nuevo tratamiento aprobado por la FDA para ayudar a los pacientes con infarto de miocardio muy grave.
Adquiere Mobilize Rescue Systems™, que ofrece sistemas interactivos para atender traumatismos que ayudan a los testigos a salvar vidas en emergencias médicas.

Cambia el nombre de la solución Payor Logic por ZOLL AR Boost™ para reflejar mejor el posible efecto de esta tecnología en un segmento más amplio del mercado sanitario.
ZOLL completa la adquisición de Cardiac Science.
2020
La FDA aprueba el sistema de última generación TherOx, destinado a pacientes con infarto de miocardio con elevación del segmento ST con implicación de la arteria descendente anterior izquierda.
2021
Adquiere Respicardia, Inc., un proveedor de novedosos neuroestimuladores implantables para el tratamiento de la apnea central del sueño (ACS) de moderada a grave.
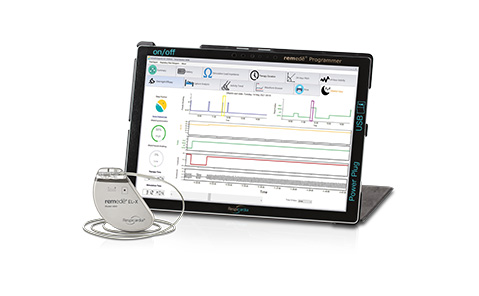
La FDA aprueba el sistema remedē® EL-X de próxima generación para tratar la ACS de moderada a grave.
Adquiere Itamar Medical, una empresa de dispositivos y salud digital que ofrece pruebas caseras para la apnea del sueño.
2022
ZOLL lanza el sistema de gestión de arritmias para planes de tratamiento más informados y añade datos biométricos a la información de telemetría cardíaca móvil tradicional.
Más de un millón de pacientes han usado LifeVest.
2023
El sistema remedē de ZOLL recibe la aprobación de la FDA para su uso condicional en la resonancia magnética, lo que da a los pacientes acceso a una gama más amplia de opciones de diagnóstico por imágenes.
ZOLL presenta el Autopulse® NXT, un avance significativo en la tecnología de RCP mecánica. El dispositivo está diseñado para realizar compresiones circunferenciales continuas en una variedad más amplia de tamaños de pacientes y, al mismo tiempo, para proporcionar una visibilidad sin obstáculos de las arterias coronarias durante la fluoroscopia en la sala de hemodinámica.